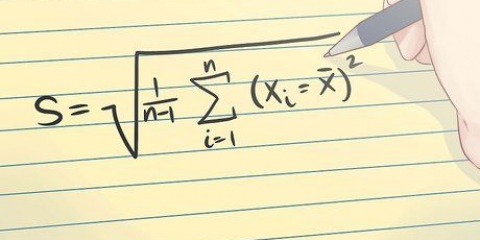Se l`ordine di legame è zero, la molecola non può formarsi. Gli ordini di legame più alti danno maggiore stabilità alla nuova molecola. 


A seconda delle dimensioni e della complessità di un particolare atomo, può avere da uno a quattro orbitali. Quando il guscio orbitale più vicino è pieno, nuovi elettroni si accumuleranno nel guscio orbitale successivo visto dal nucleo, finché anche quel guscio non sarà pieno. L`insieme degli elettroni continua in gusci orbitali sempre più grandi, perché gli atomi più grandi hanno più elettroni degli atomi più piccoli. 
La struttura di Lewis per l`azoto biatomico diventa N≡N. Ogni atomo di azoto ha una coppia di elettroni e tre elettroni non legati. Quando due atomi di azoto si incontrano, i sei elettroni non legati uniti formano un potente triplo legame covalente. 

Elettroni vincolanti: notando quanto sono pieni i gusci orbitali di ciascun atomo, puoi determinare quanti degli elettroni in uno stato energetico più elevato sono in grado di riempire i livelli di energia più stabili e inferiori dell`atomo corrispondente. Questi elettroni di "riempimento" sono indicati come elettroni di legame. Elettroni antilegame: quando due atomi cercano di formare una molecola condividendo elettroni, alcuni elettroni saranno effettivamente guidati verso gusci orbitali di livello energetico più elevato perché i gusci orbitali di livello energetico inferiore sono riempiti. Questi elettroni sono indicati come elettroni antilegame.
Calcolo dell'ordine di legame in chimica
Contenuto
A livello atomico, l`ordine di legame è il numero di coppie di elettroni legati tra due atomi. L`azoto biatomico (N≡N), ad esempio, ha ordine di legame 3 perché ci sono 3 legami chimici tra due atomi di azoto. Nella teoria degli orbitali molecolari, l`ordine di legame è anche definito come metà della differenza tra il numero di elettroni legati e non legati. Per una risposta chiara, utilizzare la seguente formula: Ordine di legame = [(numero di elettroni che legano orbitali molecolari) - (numero di elettroni negli orbitali molecolari antilegame)]/2.
Passi
Metodo 1 di 3: determinare rapidamente l`ordine del legame

1. Conosci la formula. Nella teoria degli orbitali molecolari, l`ordine di legame è definito come metà della differenza tra il numero di elettroni di legame e di antilegame. Ordine di legame = [(numero di elettroni che legano orbitali molecolari) - (numero di elettroni negli orbitali molecolari antilegame)]/2.

2. Sappi che più alto è l`ordine di legame, più stabile è la molecola. Qualsiasi elettrone aggiunto a un orbitale molecolare di legame aiuterà a stabilizzare la nuova molecola. Qualsiasi elettrone aggiunto a un orbitale molecolare antilegame destabilizzerà la nuova molecola. Scrivi il nuovo stato energetico come ordine di legame della molecola.

3. Pensa a un semplice esempio. Gli atomi di idrogeno hanno un elettrone nel S-shell e quella shell può contenere due elettroni. Quando due atomi di idrogeno si legano insieme, ciascuno riempie il S-buccia dell`altro. Si formano due orbitali di legame. Nessuno degli elettroni è costretto a spostarsi all`orbitale successivo più alto, il P-sbucciare & ndash; quindi non si formano orbitali antilegame. Quindi l`ordine del legame è  , e questo è uguale a 1. Questo forma la molecola H2: idrogeno gassoso.
, e questo è uguale a 1. Questo forma la molecola H2: idrogeno gassoso.
 , e questo è uguale a 1. Questo forma la molecola H2: idrogeno gassoso.
, e questo è uguale a 1. Questo forma la molecola H2: idrogeno gassoso.Metodo 2 di 3: Visualizzazione dell`ordine obbligazionario fondamentale

1. Determina l`ordine delle obbligazioni a colpo d`occhio. Un singolo legame covalente ha un ordine di legame di uno, un doppio legame covalente ha un ordine di legame di due, un triplo legame covalente ha un ordine di legame di tre e così via. Nella sua forma più elementare, l`ordine di legame è il numero di coppie di elettroni legati che tengono insieme due atomi.

2. Pensa a come gli atomi mettono insieme le molecole. I singoli atomi in una molecola sono legati tra loro da coppie di elettroni legati. Questi elettroni ruotano attorno al nucleo di un atomo in "orbitali" che possono contenere ciascuno solo due elettroni. Se un orbitale non è "completamente riempito", ad es., contiene solo un elettrone o nessun elettrone, quindi un elettrone non legato può legarsi con un corrispondente elettrone libero di un altro atomo.

3. Disegna le strutture di Lewis. Questo è un modo utile per visualizzare come gli atomi in una molecola sono legati insieme. Disegna gli atomi come le loro lettere (es. H per idrogeno, Cl per cloro). Indicare i titoli come linee (es., `-` per un legame singolo, `=` per un doppio legame e `≡` per un triplo legame). Contrassegna gli elettroni non legati e le coppie di elettroni come punti (esempio: C:). Dopo aver disegnato la struttura di Lewis, conta il numero di obbligazioni (l`ordine delle obbligazioni).
Metodo 3 di 3: Calcola l`ordine di legame per la teoria orbitale

1. Utilizzare un diagramma di gusci orbitali di elettroni come riferimento. Si noti che ogni guscio è sempre più lontano dal nucleo dell`atomo. Secondo l`entropia, l`energia cerca sempre di raggiungere lo stato più basso possibile. Gli elettroni cercano sempre di riempire i gusci orbitali più bassi disponibili.

2. Conoscere la differenza tra orbitali di legame e antilegame. Quando due atomi si uniscono per formare una molecola, vogliono usare gli elettroni l`uno dell`altro per riempire gli stati più bassi possibili nei gusci orbitali. Gli elettroni di legame sono essenzialmente elettroni che si uniscono e cadono nello stato energetico più basso. Gli elettroni antilegame sono gli elettroni "liberi" o non legati che vengono spinti verso livelli orbitali più elevati.
Articoli sull'argomento "Calcolo dell'ordine di legame in chimica"
Condividi sui social network:
Popolare