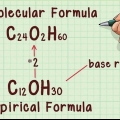
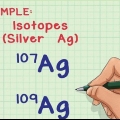
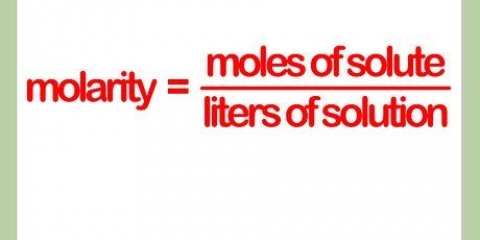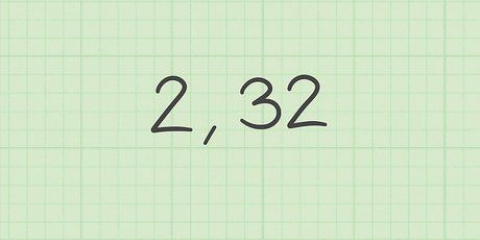Per l`anidride carbonica (CO2) la massa atomica relativa è 12.011 amu per il carbonio e 15.999 per l`ossigeno. La massa atomica di un elemento è approssimativamente uguale alla somma della massa del numero di protoni e neutroni che contiene. Nota che la massa atomica relativa che trovi nella tavola periodica è scalata: tiene conto di tutti gli isotopi dell`elemento nelle proporzioni in quanto si verificano naturalmente. 
Nel nostro esempio di anidride carbonica, la massa dell`atomo di carbonio è 12.011 amu. Poiché ci sono due atomi di ossigeno, scrivi questo come  .
. 
Arrotonda la risposta ove necessario, utilizzando cifre significative. Non dimenticare di utilizzare le unità corrette. amu è la vecchia abbreviazione per unità di massa atomica, ma un`unità migliore e moderna è una piccola scritta voi. Per l`anidride carbonica, la massa molecolare può essere trovata come segue:  .
. 





Calcolo della massa molecolare
Contenuto
La massa molecolare, precedentemente chiamata peso molecolare (MW), è la massa di tutti gli atomi in un dato formula molecolare.La massa molecolare è misurata in unità di massa atomica, solitamente espressa in voi o divertire. Per calcolare la massa molecolare di una formula, devi sommare le masse atomiche di ogni elemento presente.
Passi
Metodo 1 di 2: Calcolo della massa molecolare

1. Conta quanti atomi di ogni elemento ci sono nella molecola. Innanzitutto, elenca tutti gli elementi presenti nella molecola. Puoi usare il simbolo chimico o scrivere il nome dell`elemento. Quindi conta gli atomi secondo la formula molecolare e scrivili accanto al nome o al simbolo dell`elemento.
- Ad esempio: anidride carbonica o CO2, contiene 1 carbonio (C) e 2 ossigeno (O).
- Metano, CH4, contiene carbonio (C) e idrogeno (H). Il metano è costituito da 1 atomo di carbonio e 4 atomi di idrogeno.
- glucosio, CO6eh12o6, contiene carbonio (C), idrogeno (H) e ossigeno (O). Il glucosio è costituito da 6 atomi di carbonio, 12 atomi di idrogeno e 6 atomi di ossigeno.

2. Particolaremassa atomica relativa di ogni elemento della molecola. Usalo tavola periodica. La tavola periodica elenca la massa atomica di ciascun elemento sotto il simbolo chimico. Ad esempio: l`ossigeno ha una massa atomica relativa di 15,9994 amu.

3. Calcola la massa totale di ogni elemento nella molecola. Moltiplica la massa atomica di ciascun elemento per il numero di atomi di quell`elemento: (massa atomica dell`elemento) x (numero di atomi di quell`elemento). Fallo per ogni elemento della molecola.
 .
.
4. Somma le masse di tutti gli atomi per trovare la massa molecolare. Massa molecolare = ∑((massa atomica dell`elemento)n x (numero di atomi di quell`elemento)n)
 .
.Metodo 2 di 2: esercitati con gli esempi

1. Determinare la massa molecolare del metano (CH4). La massa atomica dell`idrogeno è 1.008 u. La massa atomica del carbonio è 12.011 u. Ci sono quattro atomi di idrogeno nel metano. Somma il peso di tutti gli atomi nel metano per trovare la massa molecolare.
.

2. Calcolare la massa molecolare del glucosio (C6eh12o6). La massa atomica del carbonio è 12.011 u. La massa atomica dell`idrogeno è 1.008 u. La massa atomica dell`ossigeno è 15.999 Ci sono 6 atomi di carbonio, 12 atomi di idrogeno e 6 atomi di ossigeno. Somma le masse di tutti gli atomi nel glucosio per calcolare la massa molecolare.




Consigli
- Assicurati di seguire le regole appropriate per le cifre significative, come richiesto.
Articoli sull'argomento "Calcolo della massa molecolare"
Condividi sui social network:
Popolare