In questa formula, n il numero di moli, P la pressione, V il volume, T la temperatura in Kelvin e R la costante del gas. Esempio: n=PV/RT=(0,984 atm x 1 L) / (0,08206 L atm mol-1 K-1 x 318,15 K)=0,0377 mol 
Esempio: 14,42 g / 0,0377 mol=382,49 g/mol 
Esempio: (12,0107 g x 12) + (15,9994 g x 1) + (1,00794 g x 30)=144,1284 + 15,9994 + 30,2382=190,366 g 
Esempio: 382.49 / 190.366=2.009 
Esempio: C12OH30 x 2=C24O2H60 

Esempio: 75,46 g C x (1 mol / 12,0107 g) = 6,28 mol C 8,43 g O x (1 mol / 15,9994 g) = 0,53 mol O 16,11 g H x (1 mol / 1,00794) = 15,98 mol H 
Esempio: la quantità molare più piccola è l`ossigeno con 0,53 mol. 6,28 mol/0,53 mol=11,83 0,53 mol/0,53 mol=1 15,98 mol/0,53 mol=30,15 
Esempio: la formula del rapporto diventa quindi C12OH30 11.83=12 1=1 30.15=30 


Determinazione della formula molecolare di una sostanza
Contenuto
La formula molecolare è un`informazione importante su una sostanza chimica. La formula molecolare indica quali atomi sono presenti nella sostanza e quanti di ciascuno. Hai bisogno della formula del rapporto per calcolare la formula molecolare e devi anche sapere che la differenza tra queste due formule è un intero.
Passi
Parte 1 di 3: Derivare la formula molecolare da una formula di rapporto

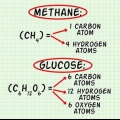
1. Conoscere la relazione tra la formula molecolare e la formula del rapporto. La formula del rapporto dice qualcosa sul rapporto tra gli atomi all`interno di una molecola, ad esempio due atomi di ossigeno su ciascun atomo di carbonio. La formula molecolare ti dice quanto di ciascuno di questi atomi è presente nella molecola. Ad esempio, un carbonio e due atomi di ossigeno (anidride carbonica). Queste due formule si relazionano tra loro di un numero intero in modo tale che se la formula del rapporto viene moltiplicata per quel rapporto, risulterà la formula molecolare.

2. Calcola il numero di moli di gas. Ciò significa che usi la legge del gas ideale. È possibile determinare il numero di moli in base alla pressione, al volume e alla temperatura forniti dai dati degli esperimenti. Il numero di moli può essere calcolato con la formula: n=PV/RT.

3. Calcola la massa molecolare del gas. Questo può essere fatto solo quando è noto il numero di moli presenti nel gas, utilizzando la legge del gas ideale. Dovrai anche sapere quanti grammi di gas sono presenti. Quindi dividere il numero di grammi di gas per il numero di moli del gas presente, per determinare la massa molecolare.

4. Somma le masse atomiche di tutti gli atomi nella formula del rapporto. Ogni atomo nella formula del rapporto ha la propria massa atomica. Questo valore può essere trovato nella parte inferiore della casella di quell`elemento, nella tavola periodica. Somma queste masse insieme per ottenere la massa della formula del rapporto.

5. Determinare il rapporto tra la massa molecolare e quella della formula del rapporto. Ciò consente di determinare la frequenza con cui la massa entra nella molecola effettiva in base alla formula del rapporto. Se lo sai, allora sai anche quante volte la formula del rapporto va nella formula molecolare. Questo dovrebbe essere un numero intero. Se il rapporto non è un numero intero, devi arrotondarlo.

6. Moltiplica la formula del rapporto per il rapporto. Moltiplica i pedici della formula del rapporto per il rapporto. Questo ti darà la formula molecolare. Si noti che per qualsiasi sostanza con un rapporto di `1`, la formula del rapporto e la formula molecolare saranno le stesse.
Parte 2 di 3: Determinazione della formula del rapporto

1. Determina la massa di ogni atomo presente. A volte verrà data la massa di ciascun atomo. In un altro momento, viene data solo la massa in percentuale. In tal caso, supponiamo che si tratti di un campione di 100 g della sostanza. Con questo puoi scrivere la percentuale di massa come massa effettiva in grammi.
- Esempio: 75,46 g C, 8,43 g O, 16,11 g H

2. Converti le masse nel numero di moli. Devi convertire la massa molecolare di ciascun elemento in mol. Per fare ciò, dividi la massa molecolare per la massa atomica di ciascun rispettivo elemento. Puoi trovare la massa atomica nella parte inferiore della casella di quell`elemento nella tavola periodica.

3. Dividi ogni valore molare per il valore molare più piccolo. Devi dividere le moli di ogni singolo elemento per la quantità molare più piccola di tutti gli elementi presenti nel composto. Ti permette di determinare i rapporti molari più semplici. Questo è valido perché l`elemento presente nella quantità minima è impostato su `1`, e fornisce le rispettive proporzioni degli altri elementi nel composto.

4. Arrotonda i valori molari a numeri interi. Questi numeri diventano i pedici della formula del rapporto. Arrotonda al numero intero più vicino. Dopo aver determinato questi numeri, puoi scrivere la formula del rapporto.
Parte 3 di 3: Comprendere la formula chimica

1. Comprendi come funziona una formula di rapporto. Una formula di rapporto fornisce informazioni sul rapporto tra un atomo e l`altro in una molecola. Questo non ti dà alcuna informazione su quanti atomi sono esattamente presenti nella molecola. La formula del rapporto inoltre non fornisce alcuna informazione sulla struttura e sul legame degli atomi in una molecola.

2. Scopri cosa ti dice una formula molecolare. Come la formula del rapporto, la formula molecolare non fornisce informazioni sul legame e sulla struttura di una molecola. Ma a differenza della formula del rapporto, la formula molecolare fornisce informazioni su quanto di ciascun atomo è presente nella molecola. La formula del rapporto e la formula molecolare si relazionano tra loro secondo un rapporto intero.

3. Comprendere le formule strutturali. Le formule strutturali forniscono ancora più informazioni rispetto alle formule molecolari. Oltre a indicare il numero di atomi in una molecola, le formule strutturali forniscono anche informazioni sui legami e sulla struttura della molecola. Questa informazione è fondamentale per capire come reagirà la molecola.
Consigli
- Leggere attentamente la dichiarazione (o i dati).
Avvertenze
- Non confondere la formula del rapporto con la formula molecolare.
Necessità
- Tavola periodica degli elementi
- Calcolatrice
- Matita
- Carta
Articoli sull'argomento "Determinazione della formula molecolare di una sostanza"
Condividi sui social network:
Simile
Popolare